Nominiert 2019
Ultra-Hochfeld-MRT

Die Antwort gaben Christina Triantafyllou, PH.D., Prof. Dr. med. Arnd Dörfler und Univ.-Prof. Dr. sc. techn. Mark E. Ladd. Dazu haben die drei Nominierten die Stärke des Magnetfelds für die MRT deutlich erhöht – und dadurch neue und detailliertere Einblicke in den menschlichen Körper ermöglicht. Durch innovative Ansätze gelang es ihnen, die Technik der Ultra-Hochfeld-MRT nicht nur für die Grundlagenforschung, sondern nun auch für den Einsatz in Kliniken zugänglich zu machen.
Christina Triantafyllou leitet den Bereich Globale Ultra-Hochfeld-Lösungen bei der Siemens Healthineers AG in Erlangen, Arnd Dörfler leitet die Abteilung Neuroradiologie am Universitätsklinikum Erlangen der Friedrich-Alexander-Universität Erlangen-Nürnberg und Mark E. Ladd ist Leiter der Abteilung Medizinische Physik in der Radiologie am Deutschen Krebsforschungszentrum Heidelberg.
"Eine Besonderheit bei der MRT ist zudem, dass man nicht nur die anatomische Information erhält, ... , sondern auch Informationen über den biologischen Zustand des Gewebes..."
Christina Triantafyllou, Ph.D.
Weitere Details
Lebensläufe
Christina Triantafyllou, Ph.D.
- 15.07.1970
- Geboren in Stuttgart, Deutschland
- 1988
- Apolytirio, High School Diploma Eniaio Polycladiko Senior High School, Katerini, Pierias, Griechenland
- 1994
- B.Sc., Physik Aristotle University of Thessaloniki, Thessaloniki, Griechenland
- 1995
- M.Sc., Medizinische Physik University of Surrey, Guildford, GB
- 1997 - 2001
- Ph.D., Medizinische Physik Institute of Psychiatry, Guy’s, King’s and St Thomas’ School of Medicine, King’s College, University of London, London, GB
- 2001 - 2006
- Harvard University, A.A. Martinos Center for Biomedical Imaging,
MRI Physics Group, Department of Radiology, Massachusetts General Hospital, Harvard Medical School, Boston, MA, USA
Promovierte, wissenschaftliche Mitarbeiterin - 2006 - 2014
- Harvard University, Department of Radiology, Massachusetts General Hospital, Harvard Medical School, Boston, MA, USA
Mitarbeiterin im Bereich Neurowissenschaften - 2006 - 2014
- Universität Harvard, A.A. Martinos Center for Biomedical Imaging, Department of Radiology, Massachusetts General Hospital, Harvard Medical School, Boston, MA, USA
Fakultät, Lehrbeauftragte - 2006 - 2012
- Massachusetts Institute of Technology (MIT), Department of Brain and Cognitive Sciences, A.A. Martinos Imaging Center, McGovern Institute for Brain Research, Cambridge, MA, USA
Leitende MRT-Physikerin - 2006 - 2012
- Massachusetts Institute of Technology (MIT), Department of Brain and Cognitive Sciences, A.A. Martinos Imaging Center, McGovern Institute for Brain Research, Cambridge, MA, USA
Wissenschaftliche Forscherin - 2012 - 2012
- Massachusetts Institute of Technology (MIT), Department of Brain and Cognitive Sciences, A.A. Martinos Imaging Center, McGovern Institute for Brain Research, Cambridge, MA, USA
Leitende wissenschaftliche Forscherin - 2007 - 2012
- Massachusetts Institute of Technology (MIT), Department of Brain and Cognitive Sciences, A.A. Martinos Imaging Center, McGovern Institute for Brain Research, Cambridge, MA, USA
Stellvertretende Direktorin - 2012 - 2013
- Siemens AG, Healthcare Sector, Business Line Magnetic Resonance Imaging Erlangen, Deutschland Leiterin, Global Ultra High Field Business Management
- 2013 - 2018
- Siemens Healthineers, Business Line Magnetic Resonance Erlangen, Deutschland Leiterin, Global Ultra High Field Product Relationship Management
- Seit 2018
- Siemens Healthineers, Business Line Magnetic Resonance Erlangen, Deutschland Solution Owner, Product Line Research and Clinical Translation
- Seit 2018
- Siemens Healthineers, Business Line Magnetic Resonance, Erlangen, Deutschland
Leiterin, Global Ultra-High Field Magnetic Resonance Solutions
Teamleiterin, Solutions and Digital, Product Line Research and Clinical Translation
Weitere Aktivitäten
- 38 von Experten begutachtete Veröffentlichungen in wissenschaftlichen Zeitschriften
94 wissenschaftliche Zusammenfassungen in Tagungsberichten
Co-Autorin von zwei Buchkapiteln
Mehr als 25 Einladungen zu Diskussionen bei internationalen wissenschaftlichen Gesellschaften und Universitäten
Ad-hoc-Gutachterin für mehrere wissenschaftliche Zeitschriften und Berufsverbände
Gutachtertätigkeit für Fördergelder (Department of Veterans Affairs, Rehabilitation R&D Study Section, Grant Review Panel, Washington DC, USA, 2011)
Mitglied in wissenschaftlichen Berufsverbänden (International Society for Magnetic Resonance in Medicine, European Society of Magnetic Resonance in Medicine, Organization for Human Brain Mapping, Institute of Physics in GB) - 1993
- Summer School in Research Advanced Physics, Department of Physics, University of Crete, Kreta, Griechenland
- 1996
- Studentische Praktikumsstelle, Nuclear Medicine Department, Hammersmith Hospital, London, GB
- 1996
- Klinische Forscherin, Nuclear Medicine Department, Leicester Royal Infirmary Hospital, Leicester, GB
- 2000 - 2001
- Wissenschaftliche Mitarbeiterin, Medical Image Processing, Robert Steiner MRI Unit, Imaging Sciences Department, Hammersmith Hospital, Imperial College, London, GB
- 2005
- Softwareentwicklerin, Austauschprogramm für Zusammenarbeit, Department of MREA, Advanced Neuro Applications Group, Siemens Healthcare, Erlangen, Deutschland
- Seit 2013
- Organisationskomitee der High Field Systems & Applications Study Group, International Society for Magnetic Resonance in Medicine (ISMRM)
- Seit 2019
- Mitglied der Gruppe “Women of ISMRM” (International Society for Magnetic Resonance in Medicine)
Ehrungen (Auswahl)
- 2010
- Infinite Mile Award for Outstanding Achievement, Office of the Provost, Office of the Vice President for Research and Associate Provost, Massachusetts Institute of Technology (MIT), Cambridge, MA, USA
- 2010
- Poster Award (1. Platz), 2. Jährliches Wissenschaftliches Symposium, Ultra High Field Magnetic Resonance: Clinical Needs, Research Promises and Technical Solutions, B.U.F.F., Berlin, Deutschland
- 1997
- Scholarship Award for Ph.D. studies, The Stroke Association, King’s College, University of London, London, GB
- Travel Stipends, International Society for Magnetic Resonance in Medicine, 13. Jahrestagung, Miami, Florida, USA, 2005, 12. Jahrestagung Kyoto, Japan, 2004, 11. Jahrestagung, Toronto, Kanada, 2003, 9. Jahrestagung, Glasgow, Schottland, GB, 2001
Travel Award, Organization for Human Brain Mapping, 6. Jahrestagung, San Antonio, Texas, USA, 2000
Travel Stipends, British Chapter of the International Society for Magnetic Resonance in Medicine, 5. Jahrestagung, London, 1999, 3. Jahrestagung, Manchester, GB, 1997
Travel Award, European Society for Magnetic Resonance in Medicine & Biology, 15. Jahrestagung, Genf, Schweiz, 1998
Forschungsinteressen
- Methodische Fortschritte in der Magnetresonanztomographie
einschließlich Bildgebung mit Ultrahochmagnetfeldern
Ultrahochauflösung in der funktionellen Magnetresonanzbildgebung
Klinische Neuroapplikationen mit Ultrahochfeld-MRT
Univ.-Prof. Dr. med. Arnd Dörfler
- 17.12.1967
- Geboren in Karlsruhe
- 1987 – 1994
- Studium der Humanmedizin an den Universitäten Heidelberg und Zürich
- 1994
- Promotion (Dr. med.)
Universität Heidelberg, Abteilung Neuroradiologie
"Magnetresonanztomographie in der Akutphase der zerebralen Ischämie - tierexperimentelle Untersuchungen an zwei Ischämiemodellen" - 2002
- Habilitation mit venia legendi
Universität Duisburg-Essen, Essen, Deutschland
Radiologische Diagnostik und experimentelle Therapie beim Mediainfarkt - 2006
- Abschluss Masterstudiengang „Management von Gesundheits- und Sozialeinrichtungen, Universität Kaiserslautern und Witten/Herdecke
- 12.1994 - 5.1995
- Abteilung Neuroradiologie, Neurologische Universitätsklinik Heidelberg
- 6.1995 - 5.1996
- Neurologische Universitätsklinik Heidelberg („klinisches Jahr“)
- 6.1996 - 6.1997
- Abteilung Neuroradiologie, Neurologische Universitätsklinik Heidelberg
- 7.1997- 11.2004
- Institut für Diagnostische u. Interventionelle Radiologie und Neuroradiologie, Universitätsklinikum Essen
- seit 12.2004
- Leitung der Neuroradiologischen Abteilung, Universitätsklinikum Erlangen
C3-Professur für Neuroradiologie, Friedrich-Alexander-Universität Erlangen-Nürnberg - seit 8.2014
- Ordinarius (W3) für Neuroradiologie, Friedrich-Alexander-Universität Erlangen-Nürnberg
- 4.2000
- Facharzt für „Diagnostische Radiologie“
- 7.2003
- Schwerpunktanerkennung „Neuroradiologie“
- 2013
- Ruf auf eine W3-Professur für Neuroradiologie an der Charité, Universitätsmedizin Berlin, nach Berufung auf W3-Professur an der FAU 7/2014 abgelehnt
- 5/2016
- Ruf auf die Professur für Neuroradiologie an der Universität Zürich, verbunden mit dem Direktorat der Klinik für Neuroradiologie am Universitätsspital Zürich (10/2016 abgelehnt)
Weitere Tätigkeiten
- mehr als 300 Veröffentlichungen in wissenschaftlichen Zeitschriften
Verfasser von 17 Buchkapiteln und 24 Übersichtsartikeln
Gutachter für über 10 wissenschaftliche Zeitschriften und eine Vielzahl nationaler (u.a. DFG) und internationaler Förderorganisationen (u.a. SNF, NHI) und Fachgesellschaften - seit 2006
- Mitglied im erweiterten Vorstand der Deutschen Gesellschaft für Neuroradiologie (DGNR)
- seit 2014
- Mitglied im Vorstand der Deutschen Gesellschaft für Neuroradiologie (DGNR)
- 2016 - 2018
- Präsident der Deutschen Gesellschaft für Neuroradiologie (DGNR)
- seit 2019
- Mitglied im Vorstand der Deutschen Röntgengesellschaft (DRG)
Forschungsschwerpunkte
- Mulimodale Bildgebungsverfahren bei neurologischen Erkrankungen
7 Tesla Hochfeld-MR-Neurobildgebung
Interventionelle Neuroradiologie
Preise/Ehrungen (Auswahl)
- 1998
- „Certificate of Excellence“ Symposium Neuroradiologicum, Philadelphia, USA
- 2002
- Kurt-Decker Preis der Deutschen Gesellschaft für Neuroradiologie
- 2006
- Felix-Wachsmann-Preis der Akademie für Fort- und Weiterbildung in der Deutschen Röntgengesellschaft
- 2010
- “Best in science” Award, Society for Vascular and Interventional Neurology, San Francisco, USA
- 2013
- Glaukomforschungspreis, Deutsche Ophthalmologische Gesellschaft
Univ.-Prof. Dr. sc. techn. Mark E. Ladd
- 07.09.1967
- Geboren in Wayne, Michigan, USA
- 1982 – 1985
- High School Diploma John Glenn High School, Westland, Michigan, USA
- 1985 – 1989
- Bachelor of Science in Engineering , University of Michigan, Ann Arbor, USA
- 1989 – 1991
- Master of Science in Electrical Engineering , Stanford University, Stanford, Kalifornien, USA
- 1995 – 1998
- Promotion (Dr. sc. techn.) Eidgenössische Technische Hochschule (ETH) Zürich, Schweiz
- 2001
- Habilitation mit venia legendi , Universität Duisburg-Essen, Essen, Deutschland
- 1986 – 1987
- General Motors Corporation, Warren, Michigan USA , Advanced Manufacturing Engineering Staff Ingenieurpraktikant
- 1989 – 1991
- Stanford University, Stanford, Kalifornien USA , Space, Telecommunications and Radioscience Laboratory Wissenschaftlicher Mitarbeiter
- 1992 – 1994
- General Electric Medical Systems, Milwaukee, Wisconsin USA Ingenieur
- 1994 – 1999
- General Electric Medical Systems in Zusammenarbeit mit dem Universitätsspital Zürich, Schweiz
Systemingenieur - 1999 – 2004
- Universitätsklinikum Essen, Deutschland
Institut für Diagnostische und Interventionelle Radiologie und Neuroradiologie
Leitender Physiker - 2000 – 2010
- MR-Innovation GmbH, Essen, Deutschland
Vizepräsident für Forschung und Entwicklung und Sicherheitsverantwortlicher - 2004 – 2013
- Universitätsklinikum Essen, Deutschland
Institut für Diagnostische und Interventionelle Radiologie und Neuroradiologie
Professor für Biomedizinische Bildgebung - 2006 – 2013
- Universität Duisburg-Essen, Essen, Deutschland
Erwin L. Hahn Institut für Magnetresonanz
Direktor - Seit 2013
- Universität Duisburg-Essen, Essen, Deutschland
Erwin L. Hahn Institut für Magnetresonanz
Principle Investigator - Seit 2013
- Universität Heidelberg, Deutschland
, Medizinische Fakultät
Professor für Medizinische Physik in der Radiodiagnostik und Biophysik - Seit 2013
- Deutsches Krebsforschungszentrum (DKFZ), Heidelberg, Deutschland
Medizinische Physik in der Radiologie
Abteilungsleiter
Weitere Tätigkeiten
- Mehr als 260 Veröffentlichungen in wissenschaftlichen Zeitschriften
Verfasser von 11 Buchkapiteln und 20 Übersichtsartikeln
Gutachter für über 20 wissenschaftliche Zeitschriften und eine Vielzahl nationaler und internationaler Förderorganisationen und Fachgesellschaften - 2010 – 2013
- Board of Trustees, International Society for Magnetic Resonance in Medicine (ISMRM)
- 2012 – 2018
- Deputy Editor der Zeitschrift „Magnetic Resonance in Medicine”
- 2013
- Guest Editor der Zeitschrift „Investigative Radiology”, Special Issue on Clinical Advances with 7 Tesla
- 2013 – 2017
- Governing Committee der High Field Systems & Applications Study Group, International Society for Magnetic Resonance in Medicine (ISMRM)
- Seit 2013
- Wissenschaftlicher Beirat „Der Radiologe“
- 2016
- Co-Vorsitzender des Workshops „UHF MRI: Technological Advances & Clinical Applications” der International Society for Magnetic Resonance in Medicine (ISMRM)
- 2017 – 2018
- Vizepräsident der Deutschen Gesellschaft für Medizinische Physik (DGMP)
- Seit 2019
- Präsident der Deutschen Gesellschaft für Medizinische Physik (DGMP)
Forschungsschwerpunkt
- Methodische Neuerungen in der Magnetresonanztomographie und Spektroskopie, einschließlich der Bildgebung mit ultrahohen Magnetfeldern, paralleler Sendeverfahren, MRT-Sicherheit und magnetresonanz-geführter Strahlentherapie
Ehrungen (ausgewählte)
- 2000
- Preisträger im Wettbewerb zur Förderung von Nachwuchsgruppen im Rahmen des Innovationsprogramms Forschung des Landes Nordrhein-Westfalen
- 2006
- Preisträger im Innovationswettbewerb zur Förderung der Medizintechnik vom Bundesministerium für Bildung und Forschung (BMBF)
- 2012
- Preisträger eines Advanced Grant des European Research Council (ERC)
Kontakt
Koordination und Pressekontakt
Ulrich Künzel
Communications, Media Relations
Siemens Healthcare GmbH
Karlheinz-Kaske-Str. 5
91052 Erlangen
Mobil: +49 (0) 162 / 24 33 492
E-Mail: ulrich.kuenzel@siemens-healthineers.com
Sprecherin
Christina Triantafyllou,Ph.D.
Siemens Healthcare GmbH
Allee am Röthelheimpark 2
91052 Erlangen
Tel.: +49 (0) 9131 / 84 54 94
E-Mail: christina.triantafyllou@siemens-healthineers.com
Beschreibung der Institute und Unternehmen zu ihren nominierten Projekten
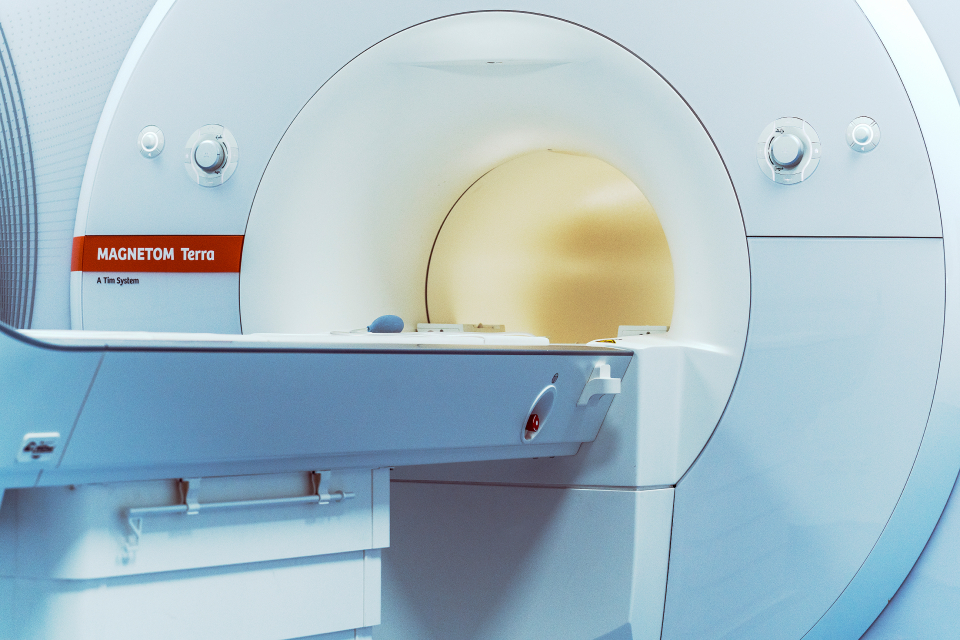
Die Magnetresonanztomographie (MRT) – auch unter dem Namen Kernspintomographie bekannt – ist mittlerweile die führende diagnostische Bildgebungsmethode und spielt bei der Diagnose einer Vielzahl von Erkrankungen eine entscheidende Rolle. Mit der Entwicklung des ersten klinischen Ultra-Hochfeld-MRT-Systems Magnetom Terra von Siemens Healthineers haben Christina Triantafyllou, Ph.D., Univ.-Prof. Dr. Mark E. Ladd und Univ.-Prof. Dr. Arnd Dörfler einen Durchbruch in der bildgebenden Diagnostik erzielt und dabei 7 Tesla als eine neue, klinische Feldstärke etabliert. Das neue System ermöglicht weltweit erstmals den Einsatz der Ultra-Hochfeld-MRT in der klinischen Anwendung. Das Forschungs- und Entwicklungsteam hat damit Neuland in der medizinischen Bildgebung beschritten und einen bedeutenden Meilenstein in der Geschichte der MRT erreicht.
Insbesondere bei Erkrankungen des zentralen Nervensystems, der inneren Organe, der Blutgefäße sowie des Bewegungsapparates bietet die 7-Tesla-MRT eine präzise Darstellung kleinster Strukturen und damit häufig die bestmögliche Diagnose. Gerade im Frühstadium von Erkrankungen wie Multipler Sklerose (MS) und neurodegenerativen Erkrankungen wie Demenz und Morbus Parkinson sind krankhafte Veränderungen häufig nicht so ausgeprägt, dass sie mit den klinisch etablierten MRT-Systemen bei geringeren Feldstärken diagnostiziert werden können. Die mit herkömmlichen MRT-Systemen erzielbare Bildqualität und räumliche Auflösung sind dafür nicht immer ausreichend. Bis zur Diagnose und dem Therapiebeginn vergeht damit oftmals wertvolle Zeit. Das Magnetom Terra von Siemens Healthineers verspricht hier eine grundlegende Verbesserung: Die Ultra-Hochfeld-Bildgebung des Magnetom Terra zeichnet sich durch einen sehr hohen Detailgrad aus und erreicht damit die Darstellung kleinster Veränderungen in der Anatomie und selbst in der Funktion von Organen. Dies unterstützt einerseits die sehr frühe Diagnosestellung und andererseits die zuverlässige Abgrenzung gegenüber anderen Erkrankungen, die mit den bisher klinisch-etablierten Feldstärken nicht realisierbar war.
Das für den Deutschen Zukunftspreis nominierte Forschungs- und Entwicklungsteam hat mit dem Magnetom Terra dafür gesorgt, dass die seit Anfang der 2000er Jahre in der Grundlagenforschung eingesetzte Ultra-Hochfeld-MRT bei einer Feldstärke von 7 Tesla seit 2017 weltweit erstmals klinischen Anwendern als neue, wirkungsvolle Diagnosemethode zur Verfügung steht – und damit auch unmittelbar den Patienten zu Gute kommt. Christina Triantafyllou leitet das globale Team „Ultra-Hochfeld-MRT-Lösungen“ bei Siemens Healthineers, Mark E. Ladd leitet die Abteilung für Medizinische Physik in der Radiologie des Deutschen Krebsforschungszentrums in Heidelberg, Arnd Dörfler leitet die Neuroradiologische Abteilung am Klinikum der Friedrich-Alexander Universität Erlangen-Nürnberg.
Neben der klinischen Einführung der Ultra-Hochfeld-MRT bei 7 Tesla, stellt das Magnetom Terra auch eine bislang nicht erreichte Ingenieursleistung dar: So wurden nicht nur neue Sicherheitskonzepte für die Anwendung am Menschen konzipiert, sondern darüber hinaus eigens ein neuartiger aktiv abgeschirmter Magnet entwickelt, der bei höherer Leistungsfähigkeit deutlich kleiner und nur halb so schwer wie die Magneten bisheriger Forschungssysteme ist. Magnetom Terra kann dadurch wesentlich leichter transportiert und insbesondere einfacher in die bestehende Infrastruktur von Krankenhäusern integriert werden. Zeitaufwändige und teure Neubauten lassen sich damit vermeiden. Eine weitere Innovation stellt die Dual-Mode-Funktionalität des Magnetom Terra dar, die es den Nutzern ermöglicht, unmittelbar zwischen klinischer Nutzung und Forschungsanwendung zu wechseln. Damit bietet das System die ideale Plattform für eine translationale Forschung – neueste Forschungsergebnisse können damit schnell auch den Patienten zu Gute kommen.
Frühzeitige Diagnose und effektivere Gegenmaßnahmen bei Multipler Sklerose
Die innovative metabolische Bildgebungstechnologie des Magnetom Terra kann krankhafte Veränderungen bereits auf Stoffwechselebene sichtbar machen, noch bevor sich diese morphologisch-anatomisch manifestieren. Dabei zeigt die Feldstärke von 7 Tesla, die etwa dem 140.000-fachen des Erdmagnetfeldes entspricht, beeindruckende Erfolge: Während es bei MS bislang nur im fortgeschrittenen Stadium möglich war, die krankhaften Veränderungen auf den klinischen Bildern zu erkennen, können diese bei 7 Tesla nicht selten bereits in der Frühphase der Erkrankung als solche erkannt und sogar kleinste Läsionen in der grauen Hirnsubstanz nachgewiesen werden. Gerade bei den oft jungen MS-Patienten ist diese frühzeitige Diagnose und der schnelle Therapiebeginn von großer Bedeutung, um im weiteren Krankheitsverlauf eine Behinderung zu verzögern oder ganz zu verhindern.[1], [2]
Präzise Identifizierung von Epilepsieherden
Epilepsie stellt eine der häufigsten neurologischen Erkrankungen dar. Allein in Deutschland leben rund eine halbe Million Epilepsiepatienten. Selbst unter bester medikamentöser Behandlung bleibt ein nicht unerheblicher Teil dieser Patienten nicht anfallsfrei, was das Leben der Betroffenen stark einschränkt. Diese Patientengruppe kann wiederum mit hoher Erfolgsquote von einem epilepsiechirurgischen Eingriff profitieren. Bei dieser werden dem Patienten Epilepsieherde im Gehirn operativ entfernt. Nach vollständiger Entfernung können die Patienten anfallsfrei leben. Durch die überragende Detailauflösung des Magnetom Terra können Epilepsieherde präziser diagnostiziert oder sogar erst als solche erkannt werden. Der Eingriff wird dadurch zuverlässiger und die Betroffenen können ihre ursprüngliche Lebensqualität zurückgewinnen.[3], [4]
Natrium-Bildgebung bei neuro-degenerativen Erkrankungen
Bei Demenzerkrankungen kann in der Regel erst im fortgeschrittenen Stadium eine Diagnose gestellt werden. Dann sind bereits morphologische Schädigungen im Gehirn entstanden. Auch hier bietet Magnetom Terra neue Möglichkeiten, Morbus Parkinson oder Morbus Alzheimer in einem frühen Stadium nachzuweisen. Die für Alzheimer typischen Ablagerungen können mit der Ultra-Hochfeld-MRT besser als zuvor dargestellt und auch bei Parkinson können Strukturveränderungen in ganz bestimmten Gehirnarealen in der Frühphase zuverlässig erkannt werden. Hier spielen anatomisch sichtbare Merkmale ebenso eine Rolle[5] wie Veränderungen im Stoffwechsel, die unter anderem durch die sogenannte Natrium-Bildgebung deutlich gemacht werden können.[6] Diese metabolische MRT-Bildgebung auf Basis von Natrium wurde weltweit erstmals 2018 mit dem Magnetom Terra für die klinische Nutzung in Europa und den USA freigegeben.
Verbessertes Therapie-Monitoring in der Onkologie
In der Onkologie bietet Magnetom Terra ebenfalls neue Möglichkeiten für eine frühere Therapie und ein besseres Monitoring. Zwar lassen sich Krebserkrankungen häufig mit den bereits in der Klinik etablierten Feldstärken diagnostizieren, bis allerdings ersichtlich ist, ob eine Therapie angeschlagen hat, können oftmals Wochen vergehen. Mit der Ultra-Hochfeld-MRT ist es in der klinischen Forschung gelungen, anhand von Biomarkern Hirntumore so zu charakterisieren, dass eine verbesserte Verlaufsprognose und damit auch eine angepasste, personalisierte Therapie möglich wird – im Sinne der Präzisionsmedizin.[7] Auch die für aggressive Tumoren typische Neugefäßbildung kann bei 7 Tesla sichtbar gemacht und klinisch in Diagnostik und Therapiemonitoring genutzt werden. Die Untersuchung von Stoffwechselvorgängen mittels spektroskopischer Verfahren sowie die Bildgebung mit Natrium eröffnen ebenfalls neue Möglichkeiten zur Charakterisierung von Tumoren.1, [8], [9]
Die Physikerin Christina Triantafyllou war eine treibende Kraft hinter der Entwicklung des Magnetom Terra, mit dem weltweit erstmals die technischen Vorrausetzungen für die klinische Anwendung der 7-Tesla-Bildgebung geschaffen wurden. Mark E. Ladd, leitender Physiker am Deutschen Krebsforschungszentrum in Heidelberg hat führend mitgewirkt, als in den 2000er Jahren die ersten 7-Tesla-MRT-Systeme für Forschungszwecke am Universitätsklinikum Essen sowie in Heidelberg installiert wurden. Auch an der klinischen Zulassung des Magnetom Terra war er maßgeblich beteiligt. Der Radiologe und Neuroradiologe Arnd Dörfler war in der Entwicklungsphase eingebunden: Er spielte insbesondere bei der klinischen Implementierung und Validierung des weltweit ersten für den klinischen Betrieb vorgesehenen 7-Tesla-MRT-Systems am Universitätsklinikum Erlangen sowie der Zulassung des Magnetom Terra eine wesentliche Rolle.
¹ Der Forschungsmodus befindet sich in der Entwicklungsphase und ist kommerziell nicht in den USA und anderen Ländern verfügbar. Die zukünftige Verfügbarkeit kann nicht garantiert werden.
Siemens Healthineers unterstützt Gesundheitsversorger weltweit dabei, auf ihrem Weg hin zu dem Ausbau der Präzisionsmedizin, der Neugestaltung der Gesundheitsversorgung, der Verbesserung der Patientenerfahrung und der Digitalisierung des Gesundheitswesens mehr zu erreichen. Als ein führendes Unternehmen der Medizintechnik entwickelt Siemens Healthineers sein Produkt- und Serviceportfolio stetig weiter. Das gilt für die Kernbereiche der Bildgebung für Diagnostik und Therapie sowie für die Labordiagnostik und die molekulare Medizin. Zusätzlich werden die Angebote im Bereich digitale Gesundheitsservices und Krankenhausmanagement gemeinsam mit den Betreibern stetig weiterentwickelt. Im Geschäftsjahr 2018, das am 30. September 2018 endete, erzielte Siemens Healthineers ein Umsatzvolumen von 13,4 Milliarden Euro und ein bereinigtes Ergebnis von 2,3 Milliarden Euro und ist mit rund 50.000 Beschäftigten weltweit vertreten. Weitere Informationen finden Sie unter www.siemens-healthineers.com.
Das Deutsche Krebsforschungszentrum (DKFZ) ist mit mehr als 3.000 Mitarbeiterinnen und Mitarbeitern die größte biomedizinische Forschungseinrichtung in Deutschland. Über 1.300 Wissenschaftlerinnen und Wissenschaftler erforschen im DKFZ, wie Krebs entsteht, erfassen Krebsrisikofaktoren und suchen nach neuen Strategien, die verhindern, dass Menschen an Krebs erkranken. Sie entwickeln neue Methoden, mit denen Tumoren präziser diagnostiziert und Krebspatienten erfolgreicher behandelt werden können. Beim Krebsinformationsdienst (KID) des DKFZ erhalten Betroffene, interessierte Bürger und Fachkreise individuelle Antworten auf alle Fragen zum Thema Krebs. Gemeinsam mit Partnern aus den Universitätskliniken betreibt das DKFZ das Nationale Centrum für Tumorerkrankungen (NCT) an den Standorten Heidelberg und Dresden, in Heidelberg außerdem das Hopp-Kindertumorzentrum KiTZ. Im Deutschen Konsortium für Translationale Krebsforschung (DKTK), einem der sechs Deutschen Zentren für Gesundheitsforschung, unterhält das DKFZ Translationszentren an sieben universitären Partnerstandorten. Die Verbindung von exzellenter Hochschulmedizin mit der hochkarätigen Forschung eines Helmholtz-Zentrums an den NCT- und den DKTK-Standorten ist ein wichtiger Beitrag, um vielversprechende Ansätze aus der Krebsforschung in die Klinik zu übertragen und so die Chancen von Krebspatienten zu verbessern.
Das DKFZ wird zu 90 Prozent vom Bundesministerium für Bildung und Forschung und zu 10 Prozent vom Land Baden-Württemberg finanziert und ist Mitglied in der Helmholtz-Gemeinschaft Deutscher Forschungszentren.
Das Universitätsklinikum Erlangen umfasst mit seinen 50 Kliniken, selbstständigen Abteilungen und Instituten alle Bereiche der modernen Medizin. Die Gebäude des Uni-Klinikums liegen überwiegend zentral am Schlossgarten und beherbergen mehr als 1.350 Betten. Patientenversorgung, Forschung und Lehre sind auf modernstem Niveau miteinander verknüpft. Patienten profitieren von neuesten Behandlungsmethoden, die in vielen Fällen andernorts noch nicht zur Verfügung stehen. Im Jahr 2018 wurden über 545.000 Fälle ambulant und mehr als 65.000 stationär behandelt. Umfassende Qualitätssicherungssysteme sorgen vom Empfang bis zur Entlassung für eine optimale Versorgung. Dafür engagieren sich über 7.700 Mitarbeiter in fachübergreifenden Teams. Alle haben ein gemeinsames Ziel: Leiden zu lindern und Krankheiten zu heilen.
Das Vorschlagsrecht zum Deutschen Zukunftspreis obliegt den führenden deutschen Einrichtungen aus Wissenschaft und Wirtschaft sowie Stiftungen.
Das Projekt „Ultra-Hochfeld-MRT – Präzisionsmedizin zum Wohl der Patienten“ wurde vom BDI Bundesverband der Deutschen Industrie e. V. eingereicht.
Quellenverzeichnis
[1] Springer E, Dymerska B, Cardoso PL., Robinson SD, Weisstanner C, Wiest R, Schmitt B, Trattnig S (2016): Comparison of Routine Brain Imaging at 3 T and 7 T. Invest Radiol. 51(8), p. 469-82: https://www.ncbi.nlm.nih.gov/pubmed/26863580.
[2] Obusez EC, Lowe M, Oh SH, Wang I, Jennifer Bullen, Ruggieri P, Hill V, Lockwood D, Emch T, Moon D, Loy G, Lee J, Kiczek M, Manoj Massand, Statsevych V, Stultz T, Jones SE (2018): 7T MR of intracranial pathology: Preliminary observations and comparisons to 3T and 1.5T. Neuroimage, 168, p. 459-476: https://www.ncbi.nlm.nih.gov/pubmed/27915116.
[3] Davis KA, Nanga RP, Das S, Chen SH, Hadar PN, Pollard JR, Lucas TH, Shinohara RT, Litt B, Hariharan H, Elliott MA, Detre JA, Reddy R. (2015): Glutamate imaging (GluCEST) lateralizes epileptic foci in nonlesional temporal lobe epilepsy. Sci Transl Med, 7(309):309ra161: https://www.ncbi.nlm.nih.gov/pubmed/26468323.
[4] Veersema TJ, Ferrier CH, van Eijsden P, Gosselaar PH, Aronica E, Visser F, Zwanenburg JM, de Kort GAP, Hendrikse J,
Luijten PR, Braun KPJ (2017): Seven tesla MRI improves detection of focal cortical dysplasia in patients with refractory focal epilepsy. Veersema. Epilepsia Open, 2(2), p. 162-171: https://www.ncbi.nlm.nih.gov/pubmed/29588945.
[5] Schmidt M, Engelhorn T, Marxreiter F, Winkler J, Lang S, Kloska S, Goelitz P, Doerfler A (2017): Ultra high-field SWI in the substantia nigra at 7T: reliability and consistency of the swallow-tail sign. BMC Neurology 17:194: https://www.ncbi.nlm.nih.gov/pubmed/29073886.
[6] E.A. Mellon, D.T. Pilkinton, C.M. Clark, M.A. Elliott, W.R. Witschey 2nd, A. Borthakur, R. Reddy (2009): Sodium MR imaging detection of mild Alzheimer disease: preliminary study. AJNR 30(5):978-984: https://www.ncbi.nlm.nih.gov/pubmed/19213826.
[7] Choi C, Ganji SK, DeBerardinis RJ, Hatanpaa KJ, Rakheja D, Kovacs Z, Yang XL, Mashimo T, Raisanen JM, Marin-Valencia I, Pascual JM, Madden CJ, Mickey BE, Malloy CR, Bachoo RM, Maher EA (2012): 2-hydroxyglutarate detection by magnetic resonance spectroscopy in subjects with IDH-mutated gliomas. Nature Medicine volume 18, p. 624–629: https://www.ncbi.nlm.nih.gov/pubmed/22281806.
[8] Paech D, Windschuh J, Oberhollenzer J, Dreher C, Sahm F, Meissner
JE, Goerke S, Schuenke P, Zaiss M, Regnery S, Bickelhaupt S, Bäumer P, Bendszus M, Wick W, Unterberg A,
Bachert P, Ladd ME, Schlemmer HP, Radbruch A. (2018): Assessing the predictability of IDH mutation and MGMT methylation status in glioma patients using relaxation-compensated multipool CEST MRI at 7.0 T. Neuro Oncol 20(12):1661-1671: https://www.ncbi.nlm.nih.gov/pubmed/29733378.
[9] Biller A, Badde S, Nagel A, Neumann JO, Wick W, Hertenstein A, Bendszus M, Sahm F, Benkhedah
N, Kleesiek J. (2016): Improved Brain Tumor Classification by Sodium MR Imaging: Prediction of IDH Mutation Status and Tumor Progression. AJNR 37(1):66-73: https://www.ncbi.nlm.nih.gov/pubmed/26494691.
Präsentation des Projektes Abendveranstaltung, 12. September 2019


 Gebärdensprache
Gebärdensprache
 Leichte Sprache
Leichte Sprache